ربما سمعت عن الجينات وكيف أنك حصلت على لون شعرك من أحد الوالدين البيولوجيين ولون عينيك من الآخر. ولكن هناك ما هو أكثر من ذلك بكثير فيما يخص علم الوراثة وكيف تعمل الجينات في الجسم.
دعنا نلقي نظرة أقرب على دليل التعليمات الخاص بجسم الإنسان
الجينات هي قطع من الحمض النووي الريبوزي منقوص الأكسجين (DNA)

الدور الأساسي للجينات هو التزويد بالتعليمات لصنع البروتينات. البروتينات هي اللبنات الأساسية للجسم وتخدم وظائف مهمة مثل إصلاح الأنسجة والمساعدة في تجلط الدم.
الجينات هي قطع من الحمض النووي الريبوزي منقوص الأكسجين (DNA)
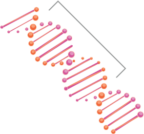
فكر في الـ DNA باعتباره اللغة المستخدمة في التعليمات الوراثية الخاصة بك. يتكون الـ DNA من مكونات تُسمَّى قواعد النيوكليوتيدات التي تشبه حروف كلمة. يجب أن يكون لديك قواعد النيوكليوتيدات الصحيحة بالترتيب الصحيح للجين لتحقيق الغرض المقصود منه - إنتاج بروتينات ذات وظيفة طبيعية.
الـ DNA يرمز إلى الحمض النووي الريبوزي منقوص الأكسجين. قواعد النيوكليوتيدات الـ 4 المسؤولة عن بناء الجينات هي الأدينين (A)، والجوانين (G)، والسايتوسين (C)، والثايمين (T). تقترن هذه النيوكليوتيدات مع بعضها البعض، A مع T وC مع G.
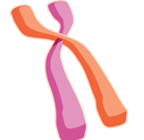
كروموسوم
يمكن العثور عليها في الكروموسومات الخاصة بنا، والتي تحتوي على عشرات الآلاف من الجينات المعروفة. تقع الكروموسومات الخاصة بك في عمق بِنية تُسمَّى النواة، والتي تعمل كمركز قيادة للخلايا التي تكوِّن جسمك.
تحتوي الخلايا البشرية عادةً على 23 زوجًا من الكروموسومات. في الذكور والإناث، 22 من هذه الأزواج تبدو متشابهة. الزوج الـ 23، والذي يُطلَق عليه أيضًا الكروموسومات الجنسية، يختلف بين الذكور والإناث. الإناث لديهم نسختان من الكروموسوم X بينما الذكور لديهم زوج واحد من الكروموسومات X وY.
هل لديك سؤال؟ كيف يمكننا المساعدة؟
يمكن أن يتسبب حدوث طفرة، أو تغير، في جين واحد فقط في حدوث حالة وراثية
هل تعلم أن هناك ما يقرب من 20000 جين في الجينوم البشري؟ يمكن أن يؤدي حدوث طفرة، أو تغير دائم، في جين واحد فقط في حدوث حالة وراثية. إن معرفة ما يُسبِّب حالة وراثية هي الخطوة الأولى في فهم كيف، من خلال البحث المستمر في العلاج الجيني، قد يكون الأطباء قادرين على علاج هذه الحالات بشكل مختلف.
الحالات الوراثية هي نتيجة للطفرات

الحالات الوراثية هي نتيجة طفرات، أو اختلافات، في بِنية جين. غالبًا ما تنتقل هذه الطفرات من الوالدين البيولوجيين ولكنها قد تحدث أحيانًا بشكل تلقائي. التلیف الكیسي الهيموفيليا مثالان على الحالات الوراثية.
في الهيموفيليا A، يتحور الجين المسؤول عن إنتاج العامل VIII. يقع هذا الجين في الكروموسوم X. الذكور لديهم فقط كروموسوم X واحد، مما يعني أن نسخة واحدة من الجين المتحور تكفي لإحداث الهيموفيليا، مما يجعلها أكثر شيوعًا في هذه الفئة المجتمعية.
في حين أنه أمر نادر الحدوث، فإن الإناث اللاتي لديهن كروموسوم واحد مصاب يمكن أن تظهر عليهن في بعض الأحيان أعراض الهيموفيليا. ولكن نظرًا لأن الإناث لديهن اثنان من الكروموسوم X، فإن كلا الكروموسومان يجب أن تكون لديهما طفرة حتى تتأثر بشدة بالمرض. ومع ذلك، فإن الإناث اللواتي لا تظهر عليهن علامات الهيموفيليا يُشار إليهن غالبًا باسم "حاملات للمرض" لأنه لا يزال بإمكانهن نقل الجين المتحور إلى أطفالهن، على الرغم من أنهن لا يعانين من أعراض الحالة.
الطفرات يمكن أن تؤثر على التعليمات الوراثية الخاصة بك
الطفرة يمكن أن تؤثر على التعليمات الوراثية في جسمك. التعليمات يمكن أن تكون مفقودة أو غير صحيحة، مما يُغيِّر طريقة إنتاج البروتينات. قد يؤدي ذلك إلى إنتاج بروتين لا يعمل بشكل صحيح أو، في بعض الحالات، لا يتم إنتاج البروتين على الإطلاق.
يمكن أن تأخذ الطفرات شكل اقتران متغير للنيوكليوتيدات، أو DNA زائد في مكان لا ينتمي إليه، أو DNA مفقود، أو DNA متكرر.
بالنسبة للأشخاص الذين يعانون من الهيموفيليا A أو B، فإن الطفرة الوراثية تؤثر على قدرة الجسم على إنتاج بروتين يُسمَّى العامل VIII أو العامل IX، على الترتيب. هذه البروتينات ضرورية لتخثر الدم.
هناك 3 أنواع من الحالات الوراثية
الأنواع الـ 3 من الحالات الوراثية هي حالات الجين الواحد، وحالات الجينات المتعددة، وحالات الكروموسومات.
- الحالات أحادية الجين—مثل الهيموفيليا- تسببها طفرة في جين واحد. وتشمل الأمثلة الأخرى التليف الكيسي و مرض هنتنغتون
- تتطور حالات الوراثة متعددة العوامل، أو حالات الجينات المتعددة، من طفرات جينية صغيرة متعددة ويمكن أن تؤدي إلى بعض الأمراض الأكثر شيوعًا التي نعرفها، مثل أمراض القلب والسكري
- تحدث اضطرابات الكروموسومات بسبب تغيرات في عدد أو هيكل الكروموسومات. متلازمة داون هي أكثر الاضطرابات شيوعًا المرتبطة بهذا النوع من الخلل
هل لديك سؤال؟ كيف يمكننا المساعدة؟
يتم تقييم حل محتمل للحالات الوراثية في تجارب سريرية متعددة لمجموعة من الحالات الوراثية لتحديد المخاطر والفوائد
الحالة الوراثية من المحتمل أن يكون لها حلاً جينيًا، هل هذا صحيح؟ أوجد هذا التفكير المنطقي أول بحث في العلاج الجيني منذ أكثر من 50 عامًا. الآن مع تقييم أبحاث العلاج الجيني في تجارب سريرية متعددة لمجموعة من الحالات الوراثية لتحديد الفوائد والمخاطر المحتملة، فإنها لديها القدرة على تقديم خيار جديد تمامًا للأشخاص الذين يعانون من حالات وراثية محددة والذين يدعمونهم ويعتنون بهم.
العلاج الجيني يهدف إلى معالجة الطفرات الوراثية

داخل خلية
ببساطة، يتم بحث العلاج الجيني في الدراسات السريرية كطريقة جديدة تحاول استخدام الجينات لعلاج الأمراض أو الوقاية منها.
يجري استكشاف طرق للعلاج الجيني
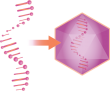
العلاج بنقل الجينات
يتم استكشاف بعض الطرق المختلفة للعلاج الجيني. قد يتضمن علاج الجينات محاولة إصلاح أو استبدال جين متحور، أو تعطيل جين متحور يسبب المتاعب، أو إدخال نسخة وظيفية من الجين في الجسم لمساعدة الجسم على إنتاج البروتین المتأثر.
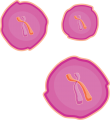
العلاج الجيني خارج جسم الحي
- مع طريقة العلاج الجيني التي تسمى نقل الجينات، يتم إدخال الجين الوظيفي في خلية بقصد أن يعمل مكان الجين المتحور. يجري استكشاف الطرق الفيروسية والكيميائية والفيزيائية لنقل الجينات. يحدث نقل الجين الجديد في الجسم (داخل الجسم الحي) بعد توصيله للجسم غالبًا باستخدام تسريب وريدي. يتم استهداف بقاء المادة الوراثية الأصلية في الكروموسومات دون تغيير. هذا يعني أن الجين المتحور سيبقى هناك ويمكن أن ينتقل إلى ذرية الشخص
- في العلاج الجيني خارج الجسم الحي، وهو نوع من العلاج القائم على الخلايا، تحدث العملية خارج الجسم. أولاً، تتم إزالة الخلايا المصابة من الجسم عن طريق خزعة. في المختبر، يتم إدخال المواد الوراثية الوظيفية في الخلايا ثم يتم توصيلها مرة أخرى إلى داخل جسم المريض

التحرير الجيني
- في التحرير الجيني، فإن الفكرة هي إجراء تغييرات على الـ DNA الأصلي. هذه التقنية تجعل من الممكن إصلاح الـ DNA الأصلي أو إضافة DNA جديد في موضع معين. نيوكلييز إصبع الزنك وCRISPR (التكرارات العنقودية المتناظرة القصيرة منتظمة التباعد) هي طرق للتحرير الجيني يجري بحثها
أكثر من 50 عامًا من البحث

تم استكشاف العلاج الجيني كمنهج علاجي محتمل لأكثر من 50 عامًا. في العقد الماضي، وافقت FDA وEMA (الوكالة الأوروبية للأدوية) على علاجات جينية للحالات الوراثية. يجري حاليًا بحث العلاج الجيني في العديد من التجارب السريرية لمختلف الاضطرابات الوراثية، بما في ذلك الهيموفيليا A وB ولم يتم بعد تحديد أنه آمن أو فعال.
لاستكشاف الأبحاث المستقبلية والحالية والسابقة في مجال العلاج الجيني، قم بزيارة ClinicalTrials.gov
الجدول الزمني للعلاج الجيني
البحوث الجارية
مازال العلاج الجيني في أبحاث تجارب سريرية مستمرة لتحديد المخاطر والفوائد المحتملة للعلاج.
هل لديك سؤال؟ كيف يمكننا المساعدة؟
تبحث البحوث الجارية عن منهج مختلف عن الطريقة التي عالجنا بها الحالات الوراثية
الأمر ليس سحرًا- إنه العلم في تقدم. العديد من العلاجات الجينية هي قيد البحث وتمت الموافقة على بعضها للاستخدام في حالات أخرى غير الهيمهوفيليا A أو B. يتم تقييم مخاطر وفوائد كل علاج جيني بشكل مستقل وإذا نجحت تجربة سريرية لعلاج جين معين، فإنها لديها الاحتمالية لتقديم منهج مختلف بشكل ملحوظ عن الطريقة التي عالجنا بها تاريخيًا الأمراض الوراثية. لنلقي نظرة على مثال…
نقل الجينات
العلاج بنقل الجينات
تهدف هذه الطريقة للعلاج الجيني، التي تمر حاليًا بتجارب سريرية في العديد من الحالات المختلفة بما في ذلك الهيموفيليا A وB، إلى إدخال جين عامل يمكن أن يعطي تعليمات للجسم لإنتاج البروتین المطلوب.
صنع جين فعال

تبدأ عملية نقل الجينات عندما يتم إنشاء نسخة فعالة من جين متحور في مختبر. يتم تطوير الجين الفعال بحيث يحتوي على تعليمات لصنع بروتين مطلوب.
بناء مركبة نقل
يوضع الـ DNA في الناقل الفيروسي
يجب الآن تسليم الجين الفعال إلى داخل الجسم. لحماية الجين والسماح بدخوله إلى الجسم، يتم صنع مركبة نقل من فيروس محايد.
تسمى مركبة النقل التي تم صنعها من فيروس محايد ناقل علاجي. يتم صنع الفيروس المحايد عن طريق إزالة المادة الفيروسية الداخلية في مختبر، تاركين وراءها غلاف بروتيني فارغ.
تشمل الفيروسات المستخدمة في نقل الجينات الفيروس الغدي، والفيروسات المرتبطة بالفيروس الغدي (AAV)، والفيروسات البطيئة. تقوم الدراسات الجارية بتقييم استجابة الجسم المناعية للعلاج الجيني.
تسليم الجين الفعال
ثم يتم وضع جين فعال داخل مركبة النقل ويتم إعطاء أعداد كبيرة منه عن طريق تسريب وريدي. بمجرد أن تحتوي مركبة النقل على جين فعال في الداخل، يُطلق عليها اسم ناقل علاجي. يتم تصميم الناقل العلاجي لتوجيه الجين الفعال نحو نسيج مُفضَّل. في الهيموفيليا A وB، يكون الكبد هو المستهدف لأنه يمكن أن يصنع البروتينات اللازمة لتجلط الدم. في أمراض أخرى، مثل مرض هنتنغتون، يكون الدماغ هو المستهدف.
عندما يتم وضع الجين الفعال داخل الـ AAV، يتم تضمين DNA إضافي يهدف إلى السماح له بالعمل وتعزيز إنتاج البروتين فقط داخل الخلايا المستهدفة. . الأبحاث مستمرة لفهم إلى أي مدى يمكن أن ينقل AAV الجين الفعال إلى أنسجة الجسم الأخرى.
صنع البروتينات

البروتينات في الجسم
بمجرد إدخاله في الجسم، فإن الجين الجديد مُصمَّم للعمل بدلاً من الجين الذي لا يعمل بشكل صحيح. إذا كان ذلك ناجحًا، فإن الهدف من هذا الجين الجديد هو توفير تعليمات للجسم لصنع البروتين الذي يحتاجه. في حالة الهيموفيليا، يتم استهداف الكبد لإنتاج البروتينات.
يدخل الجين الفعال الجديد إلى نواة الخلايا المستهدفة. هناك، من المتوقع عمومًا أن يقيم كإبيسوم أو قطعة دائرية من الـ DNA، خارج الكروموسومات. يتم استهداف بقاء المادة الوراثية الأصلية الموجودة في الكروموسومات دون تغيير. هذا يعني أن الجين المتحور سيبقى هناك ويمكن أن ينتقل إلى ذرية الشخص. في بعض الحالات، يدمج الجين مباشرةً في الـ DNA الموجود. والأبحاث مستمرة لفهم أفضل لمعدل وتأثير هذا الدمج.
يتم إجراء تجارب سريرية مستمرة لفهم كيف سيؤثر العلاج الجيني على جسم الإنسان. يُرجى التأكد من قراءة القسم "ما هي مخاطر العلاج الجيني؟"
هل لديك سؤال؟ كيف يمكننا المساعدة؟
تقوم التجارب بتقييم السلامة وما إذا كان يمكن تقليل أعباء المرض
نحن نأخذ الدواء عادةً لمساعدتنا على الشعور بشكل أفضل، سواء جسديًا أو نفسيًا. في حالة العلاج الجيني، يتم إجراء تجارب سريرية لتحديد الخطر وما إذا كان العلاج الجيني بالنسبة لبعض الأشخاص قد يخفض أو يلغي الحاجة إلى العلاج المستمر وأعباء الأمراض المزمنة. من المهم أن نتذكر أن الآثار طويلة الأجل للعلاج الجيني، بما في ذلك مدة التأثير، لا يزال يتم دراستها أيضًا ولم يتم تحديدها بعد.
إذًا، ما الذي نأمله من أبحاث العلاج الجيني؟

الجينات هي تعليمات للجسم
يهدف العلاج الجيني إلى معالجة طفرات مُعيَّنة في التعليمات الوراثية للفرد، مما يتيح للجسم إنتاج البروتينات التي يحتاجها.
إدخال الجينات الوظيفية

أحد أهداف العلاج الجيني التي يتم بحثها هو إدخال جينات فعالة في الجسم لمحاولة استهداف الطفرات المسؤولة عن الحالات الوراثية.
إنتاج البروتين

أيضًا فإن البحث هو وسيلة للجين الفعال الجديد لمساعدة الجسم على إنتاج البروتين المطلوب للعمل بشكل صحيح. على سبيل المثال، في الهيموفيليا A أو B ، فإن الهدف هو السماح للجسم بإنتاج العامل VIII أو العامل IX، على الترتيب، من تلقاء نفسه.
من المحتمل التقليل من الحاجة للعلاج

الأبحاث جارية لتحديد ما إذا كان العلاج الجيني يمكن أن يساعد الجسم على إنتاج البروتينات التي يحتاجها. قد يؤدي ذلك إلى تقليل الاعتماد على الأدوية المتوفرة حاليًا.
من المحتمل التخلص من الأعراض أو تقليلها

تقوم التجارب السريرية بتقييم ما إذا كان العلاج الجيني يمكن أن يقضي على أو يقلل من الإدارة الروتينية للأمراض. وهذا بدوره يمكن أن يقلل من العبء الجسدي والعقلي والنفسي للمرض. على الرغم من أن العلاج الجيني قد لا يكون قادرًا على معالجة الضرر الموجود مسبقًا، إلا أنه قد يكون قادرًا على تخفيف تقدم أي ضرر موجود.
كل هذه الأهداف وكذلك المخاطر يجري تقييمها حاليًا في تجارب سريرية على البشر.
هل لديك سؤال؟ كيف يمكننا المساعدة؟
تُجرى تجارب سريرية مستمرة لتحديد المخاطر المحتملة للعلاج الجيني
يتم البحث في العديد من أشكال العلاج الجيني فقط في البالغين، على الأقل في البداية، ولا تعمل بعض العلاجات الجينية في المرضى الذين لديهم أجسام مضادة معينة أو حالات أخرى موجودة سابقًا. العلاج الجيني يأتي أيضًا مع مخاطر. تُجرى تجارب سريرية مستمرة على أشخاص من فئات متعددة، لتحديد المخاطر المحتملة للمعالجة بالعلاج الجيني.
السلامة هي أولوية قصوى
من المهم فهم أن العديد من احتياطات السلامة يتم اتخاذها أثناء تطوير العلاج الجيني. تتم مراقبة التجارب السريرية في الولايات المتحدة عن كثب من قِبل إدارة الغذاء والدواء الأمريكية والمعاهد الوطنية للصحة. استنادًا إلى تقييم أجرته إدارة الغذاء والدواء الأمريكية (FDA)، فإنه يوجد أكثر من 800 دواء جديد قيد البحث من أدوية العلاج الجيني النشط مسجلة لدى إدارة الغذاء والدواء الأمريكية حاليًا. سلامة المرضى هي الأولوية القصوى. حددت التجارب والبحوث السريرية المستمرة بعض المخاطر المرتبطة بالعلاج الجيني، وقد تكشف المزيد من البحوث والخبرات عن مخاطر إضافية غير معروفة حاليًا.
المخاطر المحتملة
قد ينطوي نقل الجينات الذي يستخدم ناقل الفَيرُوس المُرْتَبِطُ بالفَيروس الغُدِّيّ (AAV) لتسليم مواد جينية جديدة على عدة مخاطر:
- كما هو الحال مع أي فيروس، يمكن أن يستجيب الجهاز المناعي للجسم للناقل العلاجي الذي تم إدخاله حديثًا كما لو كان دخيلاً. يمكن أن يؤدي رد فعل الجهاز المناعي إلى التهابات وغيرها من المخاطر الخطيرة
- يمكن أن يجعل رد الفعل المناعي العلاج الجيني يعمل بشكل أقل فعالية، أو لا يعمل على الإطلاق. لهذا السبب غالبًا ما يتم فحص مرضى العلاج الجيني المحتملين لتحديد ما إذا كان لديهم أجسام مضادة ضد فيروس مُعيَّن
- بينما الهدف من استخدام ناقل معين هو توجيه الجين الجديد إلى نوع معين من الأنسجة، فإن الفيروسات يمكن أن تؤثر على الخلايا الأخرى التي لم تكن مستهدفة، مما قد يؤدي إلى تلف أو داء أو مرض إضافي
- بعد تسليم العلاج الجيني، يمكن إخراج جزيئات الناقل من جسم المتلقي. يُسمَّى طرح الناقل هذا الطرح للناقل، ويمكن أن يحدث عن طريق البراز والبول واللعاب وسوائل الجسم الأخرى التي يتم إخراجها. يزيد هذا الطرح من احتمالية نقل هذه المواد المتبقية إلى أفراد غير مُعالَجين (من خلال الاتصال الوثيق). ويجري حاليًا تقييم أهميته في التجارب السريرية للعلاج الجيني
- يتم تقييم ما إذا كان العلاج الجيني قد يكون له تأثير سلبي على صحة العضو أو الأنسجة المستهدفة من خلال دراسات طويلة الأجل
- قد يؤدي العلاج الجيني إلى إنتاج الكثير من البروتین يمكن أن يختلف تأثير هذا الإنتاج الزائد، أو الإفراط في التعبير، بناءًا على نوع البروتين الذي يتم صنعه
- بالنسبة لبعض المرضى، قد لا يعمل العلاج الجيني على الإطلاق. وليس من الواضح حتى الآن كم من الوقت قد تستمر آثار العلاج الجيني
نحن نأمل أنك تفهم الآن بشكل أفضل علم العلاج الجيني
إنه وقت مثير بالنسبة للعلم والأمور تتغير كل يوم. التسجيل وسنكون متأكدين من استمرار الحوار.
هل لديك سؤال؟ كيف يمكننا المساعدة؟
هل تريد أخبار العلاج الجيني ومعلومات عن الحدث؟
دعنا ن HemDifferently، معًا
جزء من فعل الأشياء بطريقة مختلفة يعني وجود اتصال مفتوح. سجِّل للحصول على معلومات حول الوقائع القادمة، والموارد الجديدة، والأحدث في العلاج الجيني.
شكرًا لك!
سنكون على اتصال قريبًا.
